在上篇中,来自Nimbus和Schrödinger的科学家利用基于FEP+的策略对TYK2抑制剂展开了探索。不过,随着新发现的涌现,研发方向和策略出现了调整。
借助FEP+从头核心设计与虚拟筛选实现向TYK2 JH2变构结构域的转向
百时美施贵宝(Bristol Myers Squibb)科学家的研究证实,通过靶向JH2变构位点可实现高选择性TYK2抑制。项目团队因此做出了重大决策:转向研发靶向JH2调控结构域的TYK2抑制剂。
基于生物学验证研究,加之TYK2和JAK家族假激酶结构域的深度结构数据支持,团队得以采用多维度的、基于结构的设计策略。
研究人员利用FEP+引导化合物设计策略,通过从头核心结构探索,成功识别出吡唑并吡啶(pyrrazolono-pyridine)和吡啶并咪唑(pyridino-imidazole)核心结构(如下图),这些结构显示出良好的效力和结构域选择性,但存在多项ADME相关缺陷。
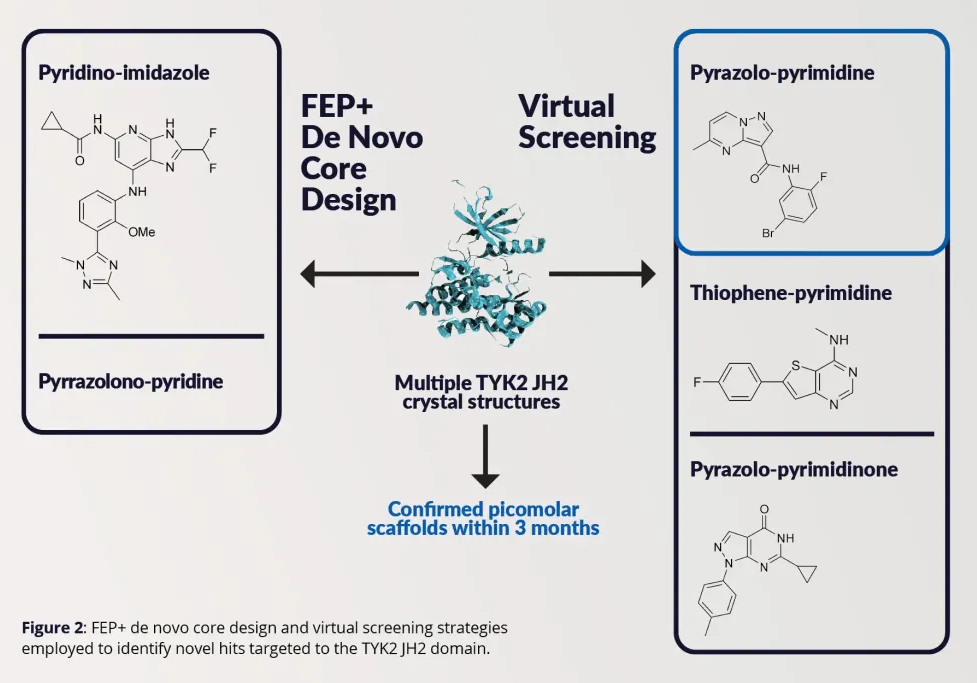
图注:FEP+从头核心设计与虚拟筛选策略
通过大规模基于结构的虚拟筛选,利用Glide(分子对接工具)和WScore(基于水网络分析的对接和评分系统),针对基于PDB数据库中已知JH2晶体结构构建的受体模型集合,对240万个市售化合物进行了筛选,最终获得3类结构不同的苗头化合物(如下图)。
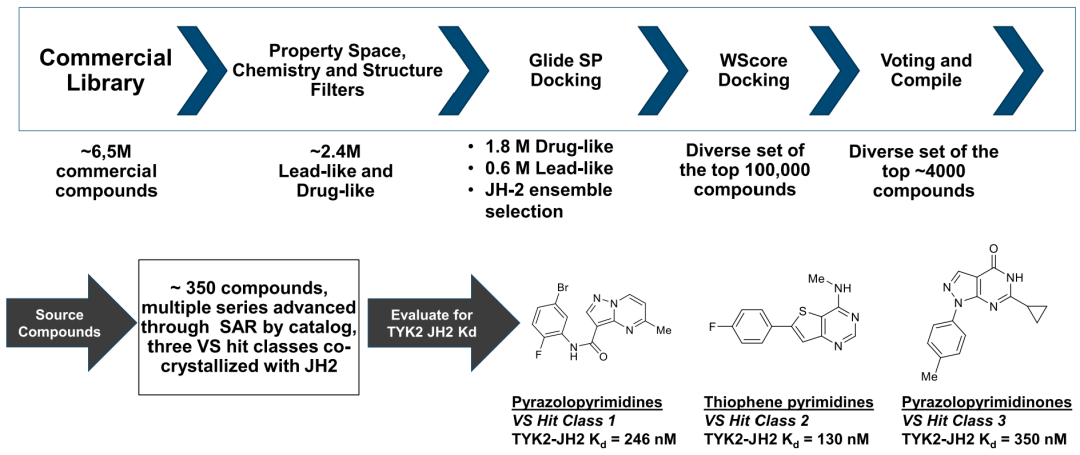
图注:用于识别TYK2 JH2结构域新型苗头化合物的虚拟筛选初筛方案
每个苗头化合物均显示出一定的JH2亲和力,其中吡唑并嘧啶(pyrazolo-pyrimidine)核心因与BMS公布的咪唑并哒嗪(imidazopyridazine)核心在空间结构和电子性质上具有相似性,被选为进一步研究的对象。通过这些基于结构的设计工作,团队在3个月内就从苗头化合物中识别出多个皮摩尔级JH2骨架结构。
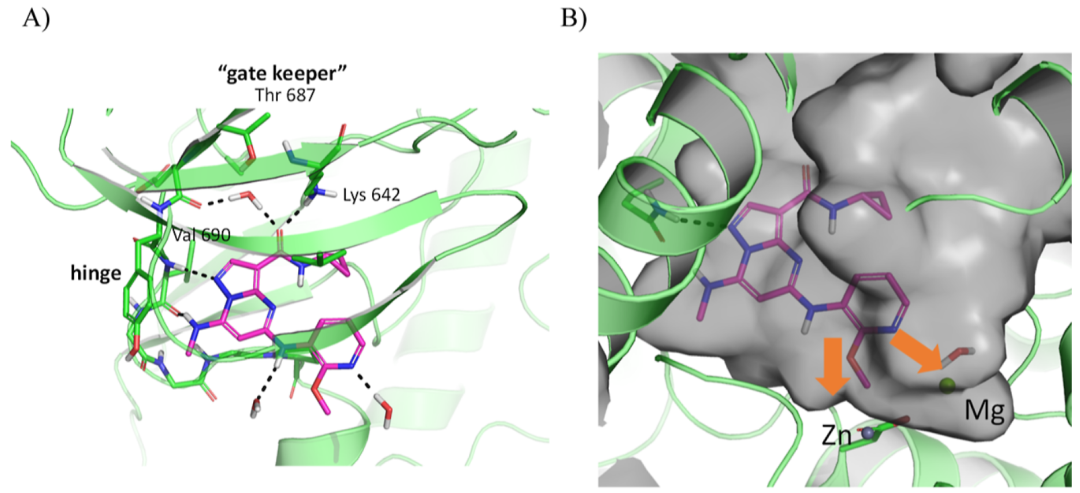
图注:化合物8(含甲氧基吡啶)与TYK2 JH2结构域结合的X射线共晶结构,揭示了吡唑并嘧啶系列苗头化合物与该蛋白假激酶结构域的关键相互作用
为推进这些苗头化合物的研发,团队再次采用了多参数优化模式与大规模建模,分为两个阶段进行:首先,对物理化学性质及被动渗透性进行快速建模,确保化合物能够进入资源密集型FEP+模型构建阶段,并保证合成是在合理的化学空间内;然后,化合物经过严格的FEP+效力预测(如下图),目标是达到皮摩尔级效力。
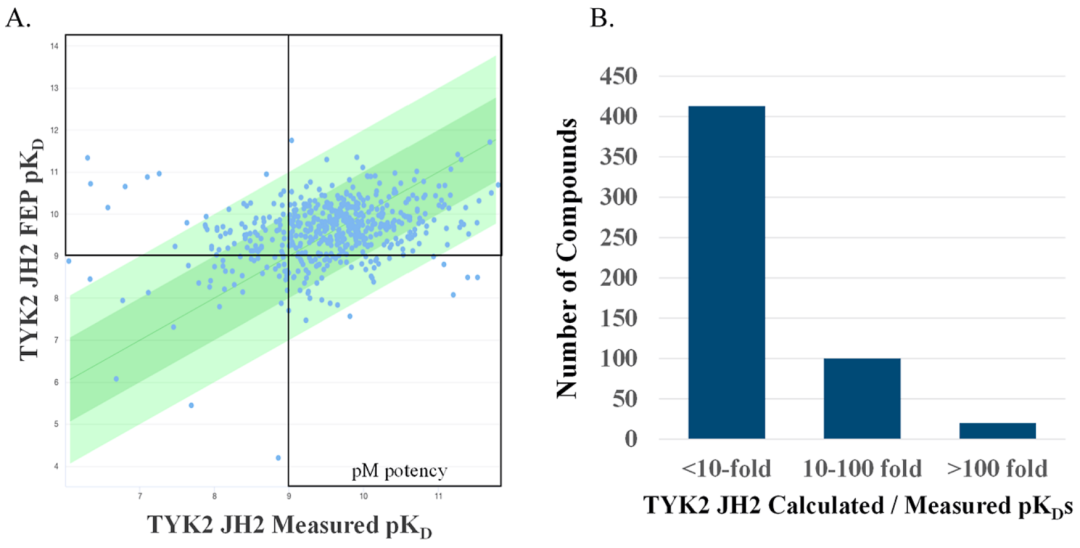
图注:针对吡唑并嘧啶系列化合物,利用FEP+技术对TYK2 JH2结合结构域进行前瞻性效力预测
所有模型和多参数优化数据均整合到云平台LiveDesign中,按不同设计目标分类到相应的LiveReports,供团队成员同步审阅。利用多参数优化策略,团队同时针对TYK2 JH2及其他JAK家族激酶结构域进行配体FEP+建模,以设计出具有高JH2亲和力和JAK家族结构域选择性的类似物。
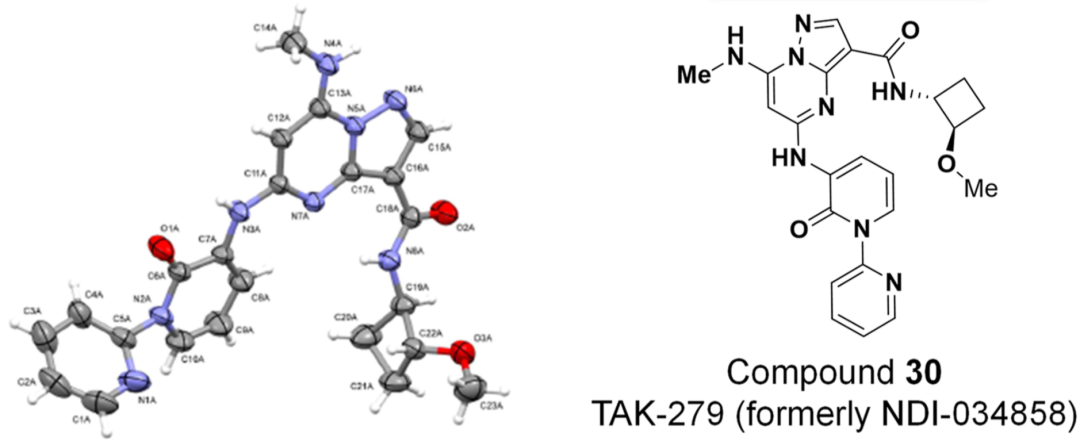
图注:化合物30的X射线晶体学展示及化学结构
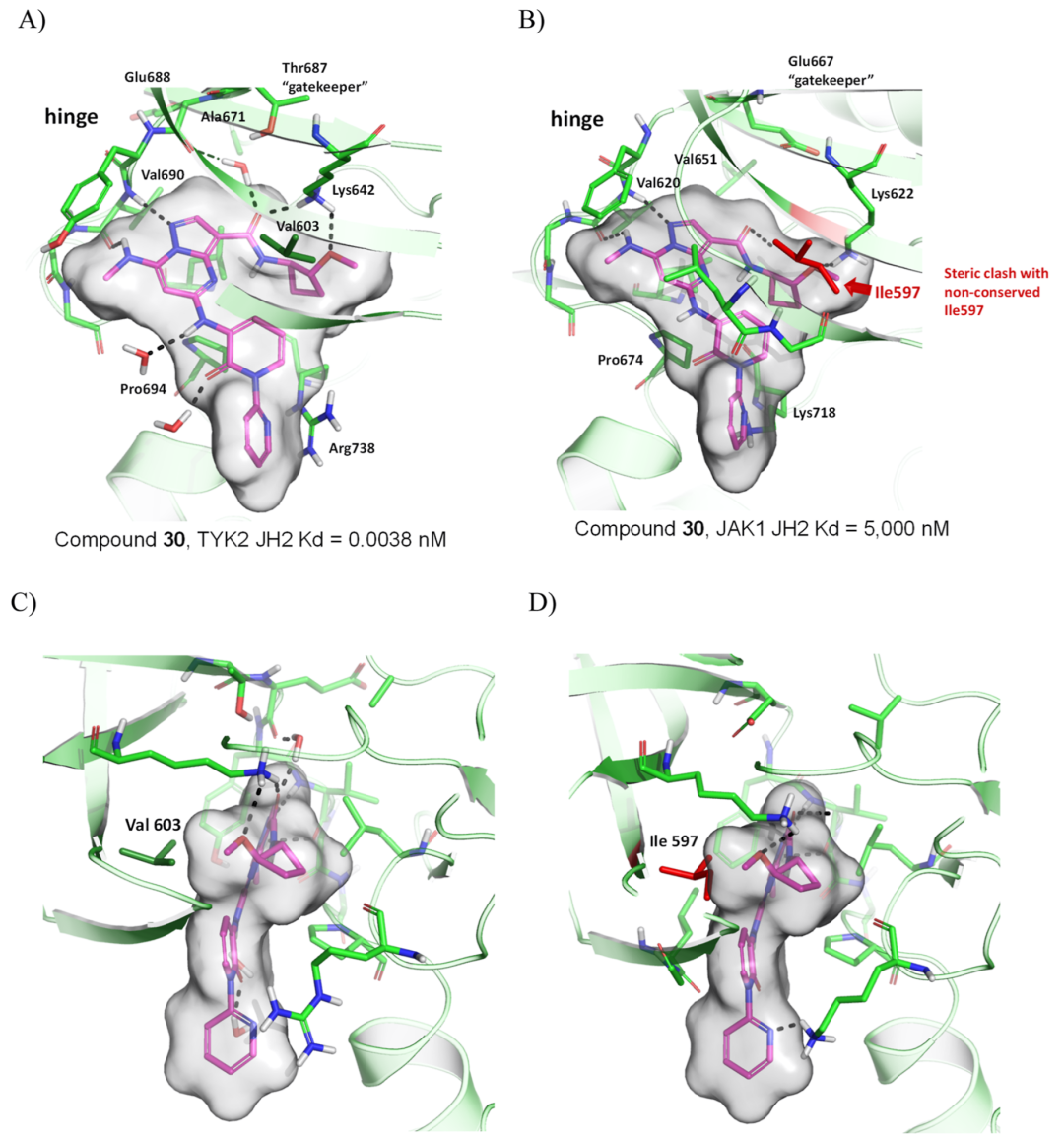
图注:化合物30对TYK2的抑制作用相较于对JAK1和JAK2的抑制具有高选择性的结构层面的机制
在转向变构TYK2项目后的两年内,团队发现了候选药物(化合物30,研发代号NDI-034858)。NDI-034858是一种经精准优化的皮摩尔级抑制剂,特异性靶向TYK2的JH2结构域,其极高的选择性已通过实验验证(如下图)。

图注:NDI-034858(TAK-279)的体外效力和脱靶选择性
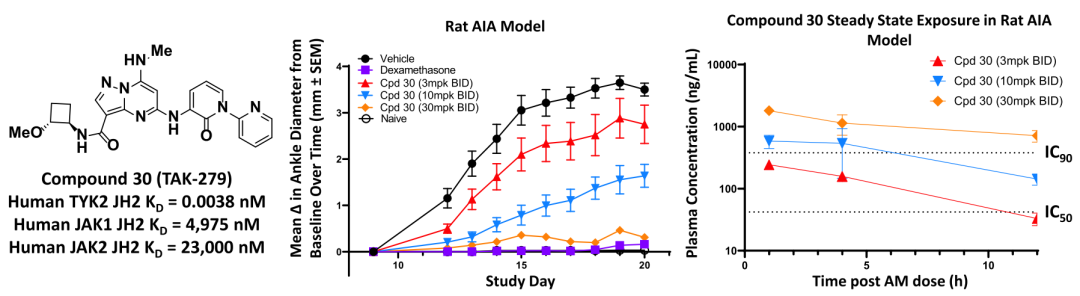
图注:TAK-279优越的体内特性
TAK-279的后续开发
2022年11月,Nimbus公布了NDI-034858用于银屑病治疗的2b期临床试验阳性顶线结果。
2023年2月,武田制药(Takeda)收购了该项目。该高选择性口服TYK2抑制剂的研发代号后更改为TAK-279,药品通用名Zasocitinib(扎索替尼),在变构抑制剂中具有同类最佳(best-in-class)潜力,可用于治疗银屑病及其他多种免疫相关的疾病。
2025年12月,武田制药公布了Zasocitinib里程碑式的3期斑块型银屑病数据,结果显示每日一次口服方案有望帮助患者实现皮损清除。武田制药计划2026年向美国食品药品监督管理局(FDA)及其他监管机构递交新药上市申请(NDA)。
总之,通过虚拟筛选、FEP+效力与溶解度预测、计算RRCK渗透性预测模型及基于结构的药物设计(SBDD),研究人员完成了一系列强效、高选择性TYK2 JH2抑制剂的优化工作,最终发现了同类最佳TYK2抑制剂Zasocitinib。



