酪氨酸激酶2(TYK2)通过1型干扰素、白介素(IL)-12/IL-23以及IL-10家族,介导细胞因子信号传导。TYK2基因变异与炎症性疾病之间存在关联,临床证据也表明,对TYK2的选择性抑制可能产生独特的治疗效果。
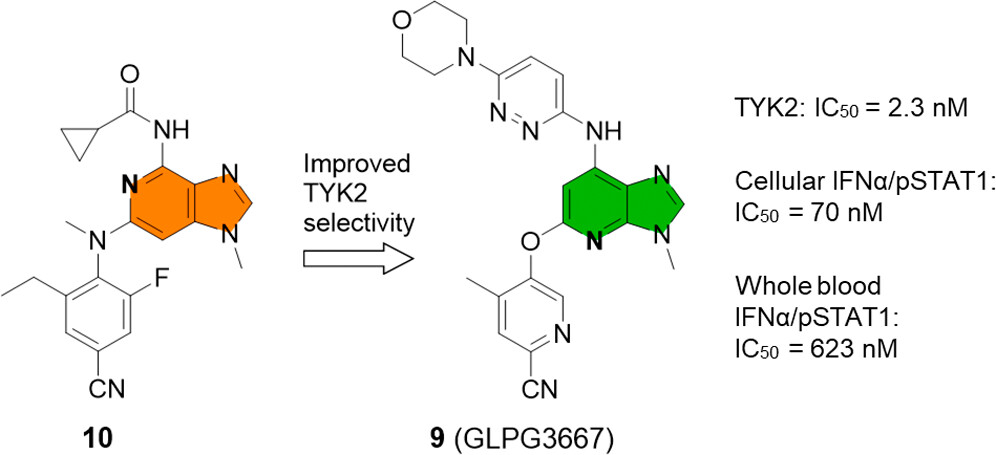
来自比利时药企Galapagos的科学家在《Journal of Medicinal Chemistry》发表了小分子药物GLPG3667(化合物9)的发现过程,这是一种可逆的、高选择性的TYK2三磷酸腺苷(ATP)竞争性抑制剂,目前正处于治疗炎症性和自身免疫性疾病的研发阶段。
图注:GLPG3667的发现
为明确化合物与TYK2的结合机制及结构差异对选择性的影响,研究人员采用Schrödinger(薛定谔)软件,通过分子配体对接、分子动力学模拟及量子力学几何优化开展了计算化学分析。
研究人员首先通过骨架跃迁设计合成了3H-咪唑并[4,5-b]吡啶系列化合物,发现了选择性较优的系列(如下图)。为阐明选择性差异的机制,后续通过分子对接开展了深入分析。
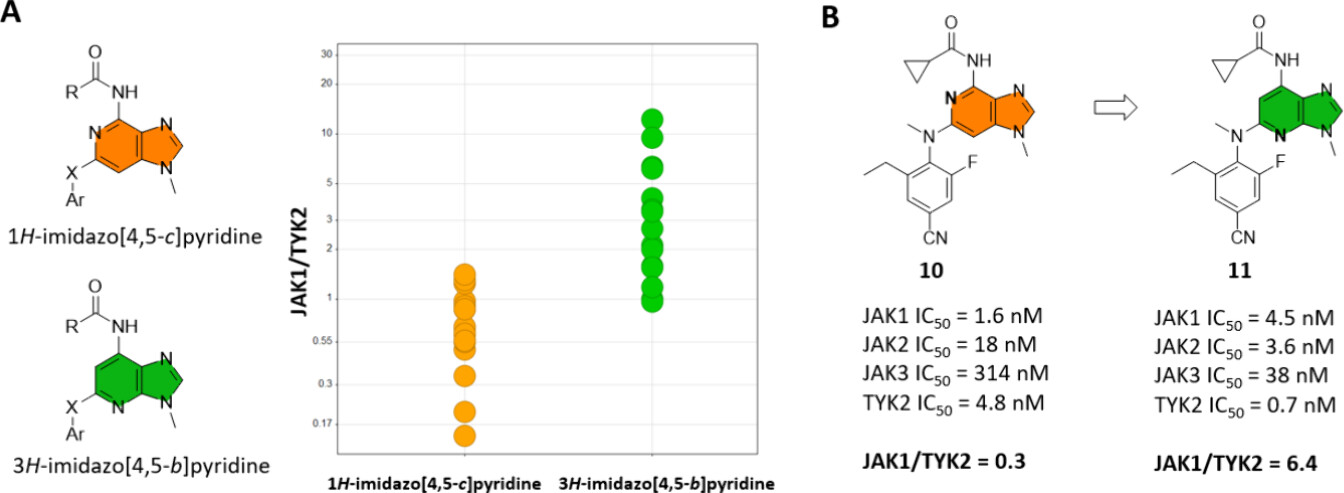
图注:A. 1H-咪唑并[4,5-c]吡啶与3H-咪唑并[4,5-b]吡啶骨架的选择性对比。B. 化合物10与11的选择性对比。
所有对接化合物均通过LigPrep构建并质子化,pH 7±2条件下的电离状态采用Epik计算。TYK2和JAK1的结构均从PDB数据库下载。
通过Protein Preparation Wizard工具为蛋白质添加氢原子。为了优化氢键网络,经可视化观察筛选残基最可能的质子化状态,并采用OPLS3力场对氢原子进行能量最小化。对接前去除了结构中所有的水分子。
分子配体对接通过Glide执行,基于预处理后的TYK2和JAK1结构生成对接网格。以共结晶配体为网格中心,设置与铰链区氢键供体(TYK2的Val981 亚氨基NH)的氢键约束,其余参数保持默认。对接过程选用灵活对接标准精度模式,同时为配体启用增强采样流程(4倍),所有对接均施加上述约束,每个配体返回5个构象。
结合模式的筛选依据包括:配体在结合腔中的空间几何结构、与口袋的互补性(形状及静电互补)、蛋白质-配体相互作用的氢键几何特征及对接得分。
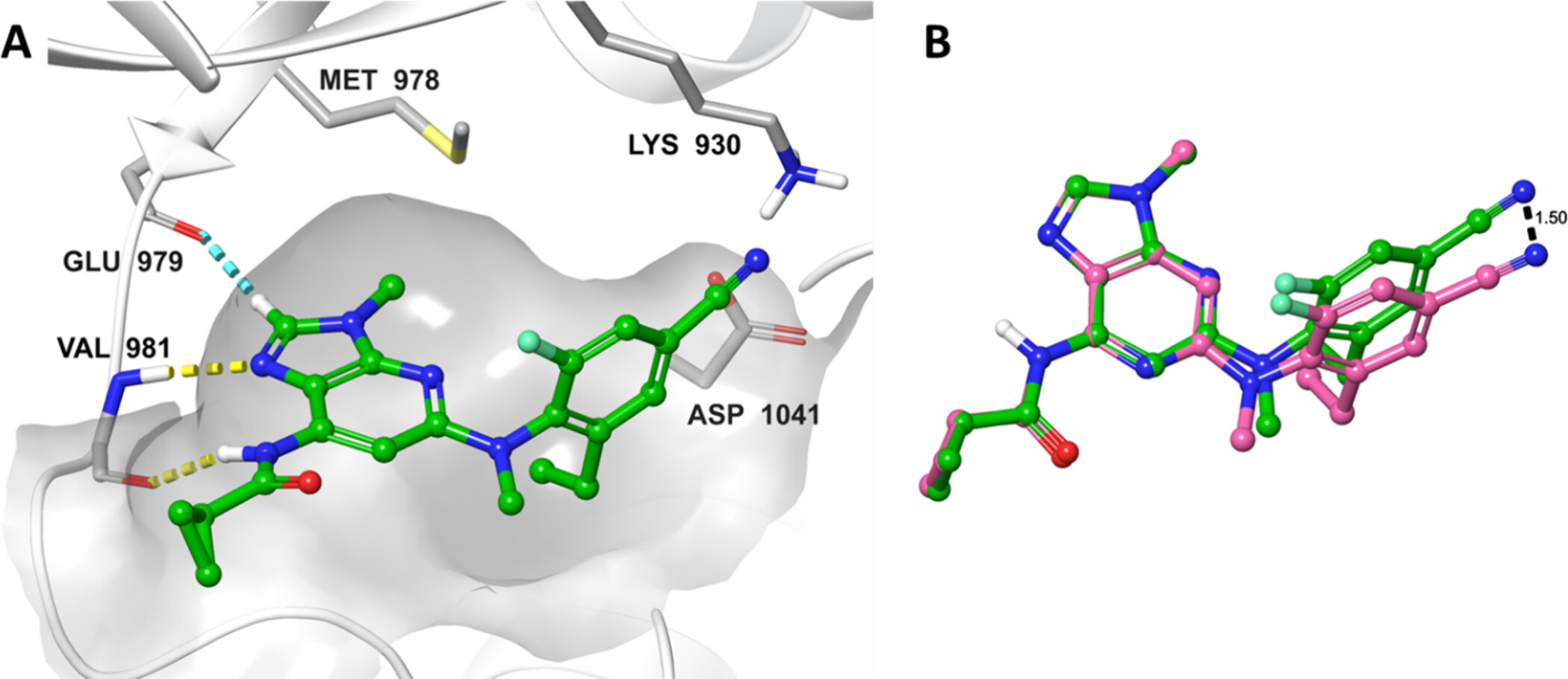
对接结果显示,化合物10和11在JAK1及TYK2结构中的结合模式极为相似(如下图)。在激酶铰链区,咪唑环氮原子与Val981的主链亚氨基NH形成氢键,而两个氮原子之间碳原子所连的氢则与Glu979的主链羰基形成弱C-H-O相互作用。
酰胺基的亚氨基NH同样与铰链区Val981的羰基氧形成氢键。氰基朝向富含甘氨酸的环,但未形成明确相互作用。乙基取代基填充于疏水口袋中。
随后,采用了Jaguar对化合物10和11在TYK2中的对接构象进行了量子力学几何优化。优化过程选用了B3LYP-D3/6-31G**泛函和基组,其余所有参数均保持默认设置。
将对接构象进行量子力学能量最小化后发现,双环核心中氮原子的位置差异导致朝向富含甘氨酸的环的芳基和氰基发生位移,这揭示了选择性提升的原因,先前研究已发现与富含甘氨酸环的相互作用是调控JAK家族选择性的关键方式。
图注:A. 化合物11对接于TYK2结构的分子模型。B. 化合物10(粉色)和11(绿色)经量子力学最小化后的结构叠加图
实用工具分享
LigPrep是一个多功能的三维分子结构生成与优化工具,用于为计算模拟准备高质量的、化学正确的配体模型。它不止是二维到三维的转换器,而是能从一个输入结构出发,生成一系列代表其化学多样性的三维结构,包括:不同的立体异构体、环构象、电离状态和互变异构体。
同时,它可以应用各种过滤规则(如分子量、官能团)来定制化合物库。LigPrep能自动纠正错误的化合价和键级,并进行能量最小化,确保输出的每一个结构在化学上和几何上都是合理的。它是进行Glide对接或Phase筛选前必不可少的配体预处理步骤,且处理速度极快。
Epik是一个用于准确快速地预测复杂类药分子水相pKa值和质子态分布的工具。利用强大的Schrödinger机器学习技术,Epik模型采用了原子图卷积神经网络集合,并在广泛的化学空间进行了训练。
分子的正确电离和互变异构状态对其与受体的结合至关重要。Epik基于经验证的Hammett-Taft方法,能够准确预测配体官能团的pKa值,并生成所有在特定pH条件下可能存在的离子化和互变异构形式。这确保了在虚拟筛选或性质预测时,使用的是生物环境中更可能存在的结构形式,从而避免因使用错误的结构而导致计算失败。
Epik与LigPrep深度整合,可以自动为整个化合物库准备正确的三维结构,是保证计算化学流程准确性的重要预处理步骤。
在明确了骨架的选择性优势后,研究团队随即开展了构效关系优化,首先聚焦于直接影响活性的C7位。那么,这一位点的修饰能否进一步提升化合物的化学特征呢?敬请关注下一篇。
欢迎联系我们获取Schrödinger软件试算!
参考资料
Mammoliti, Oscar et al. “Discovery of GLPG3667, a Selective ATP Competitive Tyrosine Kinase 2 Inhibitor for the Treatment of Autoimmune Diseases.” Journal of medicinal chemistry vol. 67,11 (2024): 8545-8568. doi:10.1021/acs.jmedchem.4c00769



