蛋白降解靶向嵌合体(PROTAC)药物因分子量大,面临透膜性差和生物利用度低等方面的挑战。
今年发表于《Cell》的一项研究采用基于生物素化学探针的靶点垂钓技术与基因敲低/敲入技术,发现CD36膜蛋白可结合多种PROTAC(如SIM1-Me、MZ1及ARV-110)以及分子量较大和/或极性较强的小分子药物,并通过CD36介导的EEA1/Rab5内体级联反应(endosomal cascade),在体外和/或体内促进这些药物的细胞摄取并提升药效。
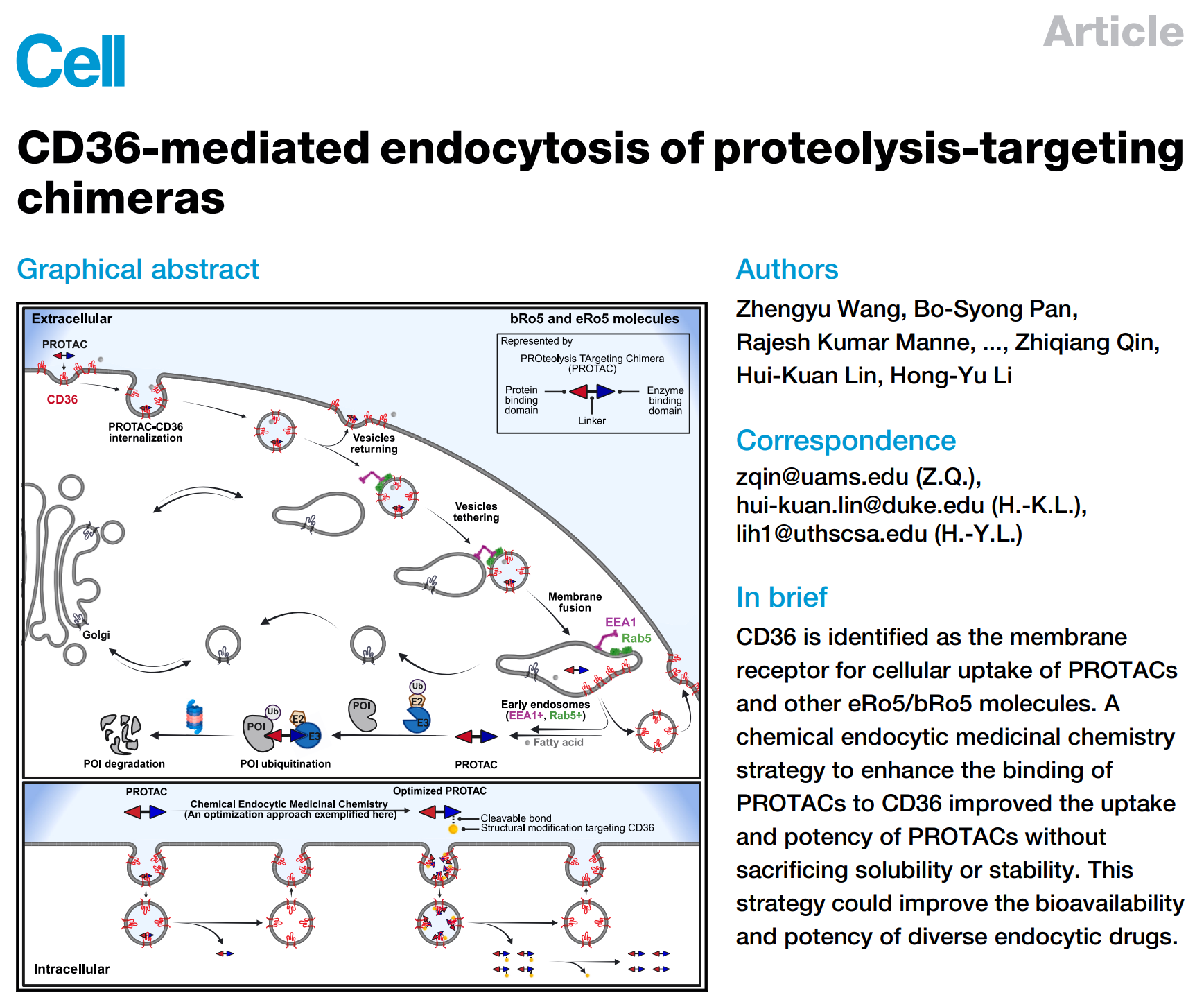
在此基础上,研究团队设计了一种全新的化学内吞药物化学策略(如下图),利用前药技术对PROTAC进行结构修饰,以此增强其与CD36的结合能力。这个策略可通过自发提升药物的渗透性与溶解度,显著增强PROTAC的抗肿瘤疗效。
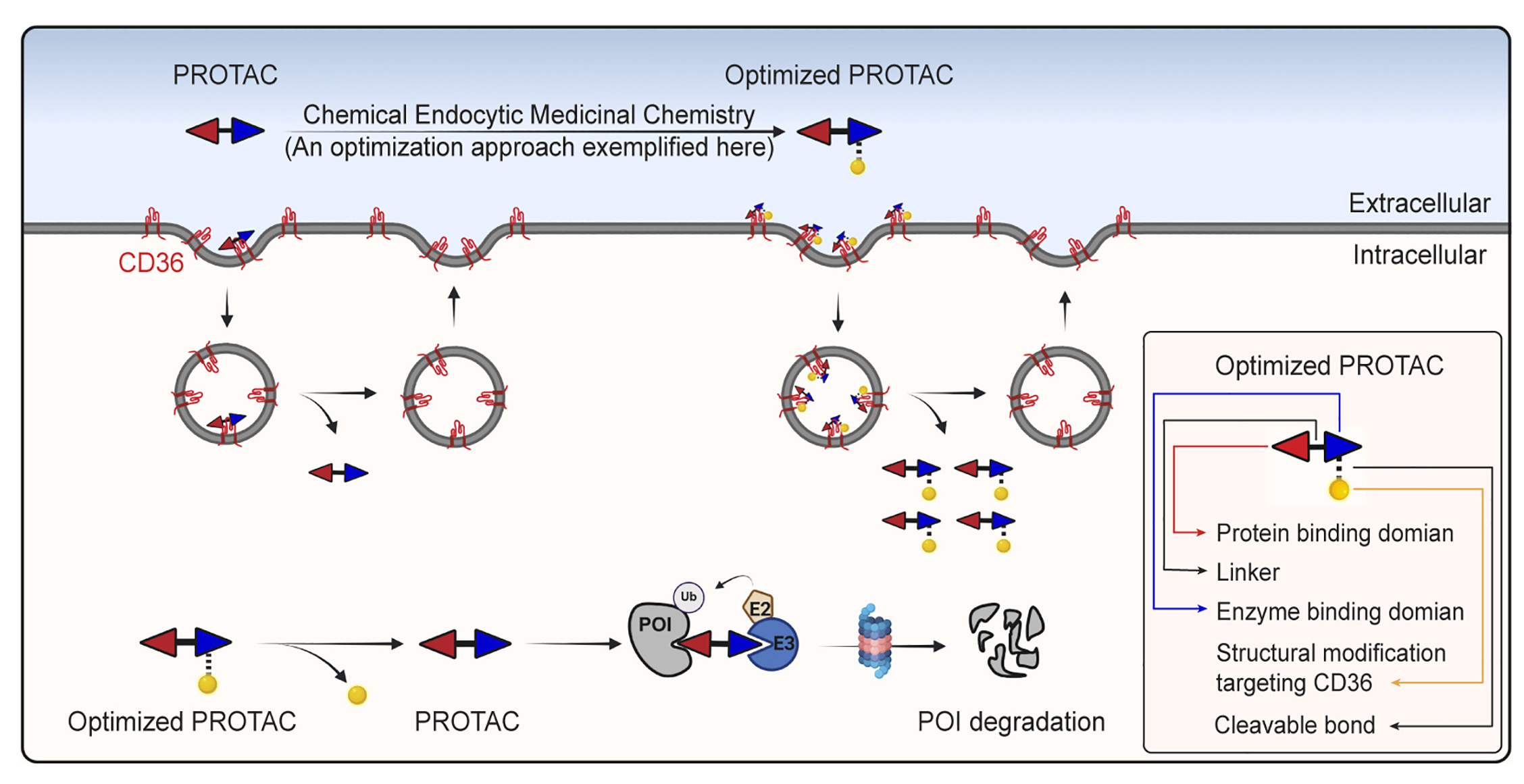
图注:MZ1的工作原理和经优化的MZ1类似物
MZ1是由BRD4配体和von Hippel-Lindau配体相连的一种新型PROTAC蛋白降解剂(如下图),具有抗肿瘤活性。为阐明人源CD36(hCD36)分别与带负电的MZ1-C14-Na和中性的MZ1-C10-NB两种化合物的潜在结合模式(二者结构基团不同,但分子尺寸相近且对CD36的亲和力相当),研究人员基于已解析的hCD36晶体结构(PDB编号:5LGD)进行了分子建模。
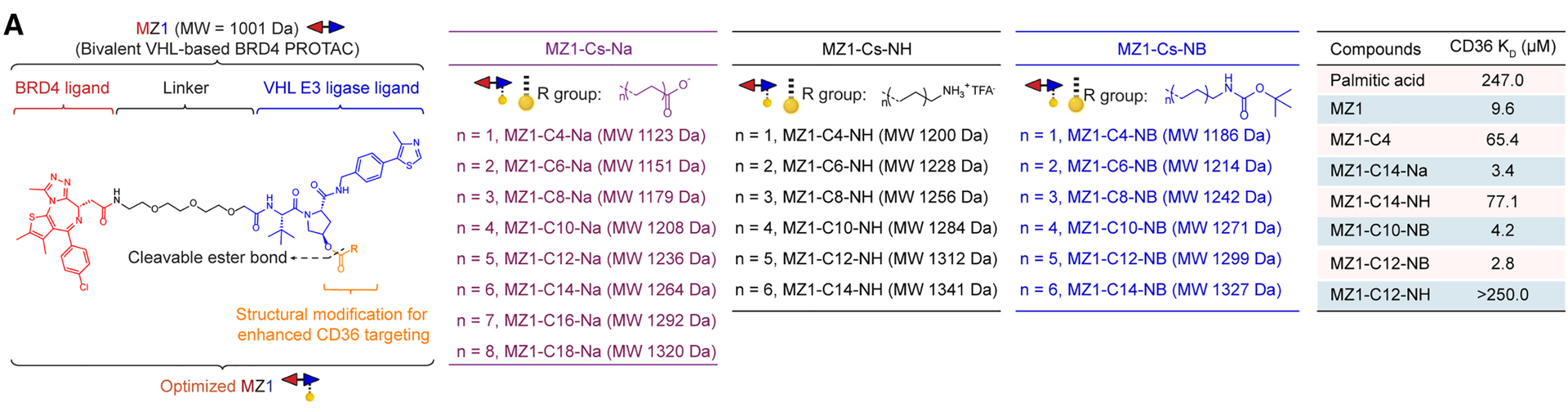
图注:基于VHL的BRD4-PROTAC MZ1和经优化的MZ1类似物的化学结构及其与CD36的结合亲和力
具体而言,获取到CIDRa结构域与CD36结合的晶体结构后,剔除了CIDRa来源的无关蛋白链及糖基。采用薛定谔(Schrödinger)的蛋白质预处理工具(Protein Preparation Wizard)对原始CD36结构进行预处理及能量最小化。同时,将配体长度的筛选范围设定为23 Å以内。
在保持化合物正确构象的前提下,利用配体预处理工具(LigPrep)完成了MZ1-C14-Na和MZ1-C10-NB两种化合物的结构准备,随后对准备完成的配体构象进行柔性对接。
结果显示,带负电荷的MZ1-C14-Na通过其羧基负离子(–COO⁻),与CD36膜远端表面的赖氨酸164残基(K164)形成了盐桥(下图C),该位点正是CD36识别长链脂肪酸的区域。
不过,MZ1-C10-NB分子中体积较大的亲脂性N-叔丁氧羰基(–N-Boc)侧链,则更倾向于通过氢键与苏氨酸195残基(T195)相结合从而占据CD36的中央空腔(下图D),而T195残基本身即为CD36中央疏水空腔内负责结合长链脂肪酸的关键位点。
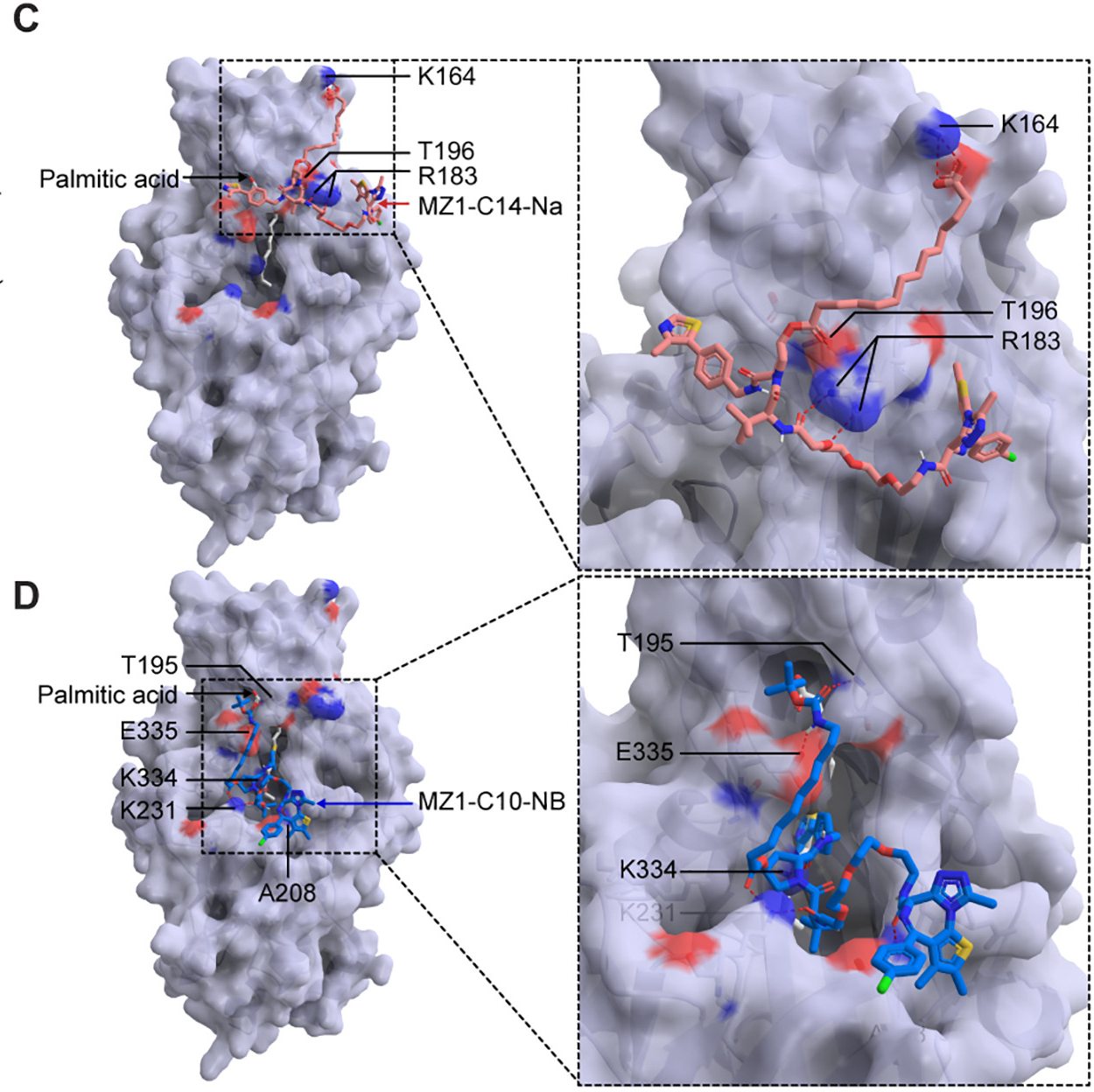
图注:人源CD36蛋白与MZ1-C14-Na(图C)及MZ1-C10-NB(图D)的分子建模
总之,研究人员采用薛定谔软件进行分子建模,为解析CD36与PROTAC的结合模式提供了支撑。薛定谔软件以精准的计算和方便的工具,加速靶点解析、药物优化,赋能结构生物学与药物研发。
欢迎联系我们获取薛定谔软件试算!
参考资料
Wang, Zhengyu, et al. "CD36-mediated endocytosis of proteolysis-targeting chimeras." Cell 188.12 (2025): 3219-3237.



