MALT1是B细胞受体信号通路中BTK下游CARD11-BCL10-MALT1(CBM)复合物的关键组成部分。它是NF-κB信号通路的关键介导因子,是非霍奇金B细胞淋巴瘤多种亚型的潜在治疗靶点。
通过应用先进的基于物理学的建模技术,包括将自由能计算与机器学习方法相结合,以及采用具有化学感知力的化合物枚举流程,研究人员探索了大量全新的药物设计思路,快速确定出新型活性化合物系列。(“化学感知力”指在人工智能及机器学习系统中内置明确的化学原理、定律和结构-属性关系知识。)
在先导化合物优化阶段,多参数优化(MPO)高效筛选出兼具良好活性和类药性的分子,最终发现了强效MALT1抑制剂——SGR-1505,其渗透性、外排性和溶解性等性质特征平衡且出色,解决了第一代MALT1抑制剂的诸多局限性。
接下来,小编将依据近期文献为您拆解SGR-1505的开发过程。

药物研发的核心挑战在于兼顾对目标靶点的亲和力,以及理想的物理化学性质。此前已有公司开发出MALT1别构抑制剂MLT-748,其与MALT1形成的共晶结构如下图所示(由Schrödinger平台的Protein Preparation Workflow构建而成)。结合口袋是一个狭窄的疏水性通道,位于半胱天冬酶结构域与Ig3结构域的交界处。基于此,如何设计出高活性、高选择性且可口服的MALT1别构抑制剂呢?
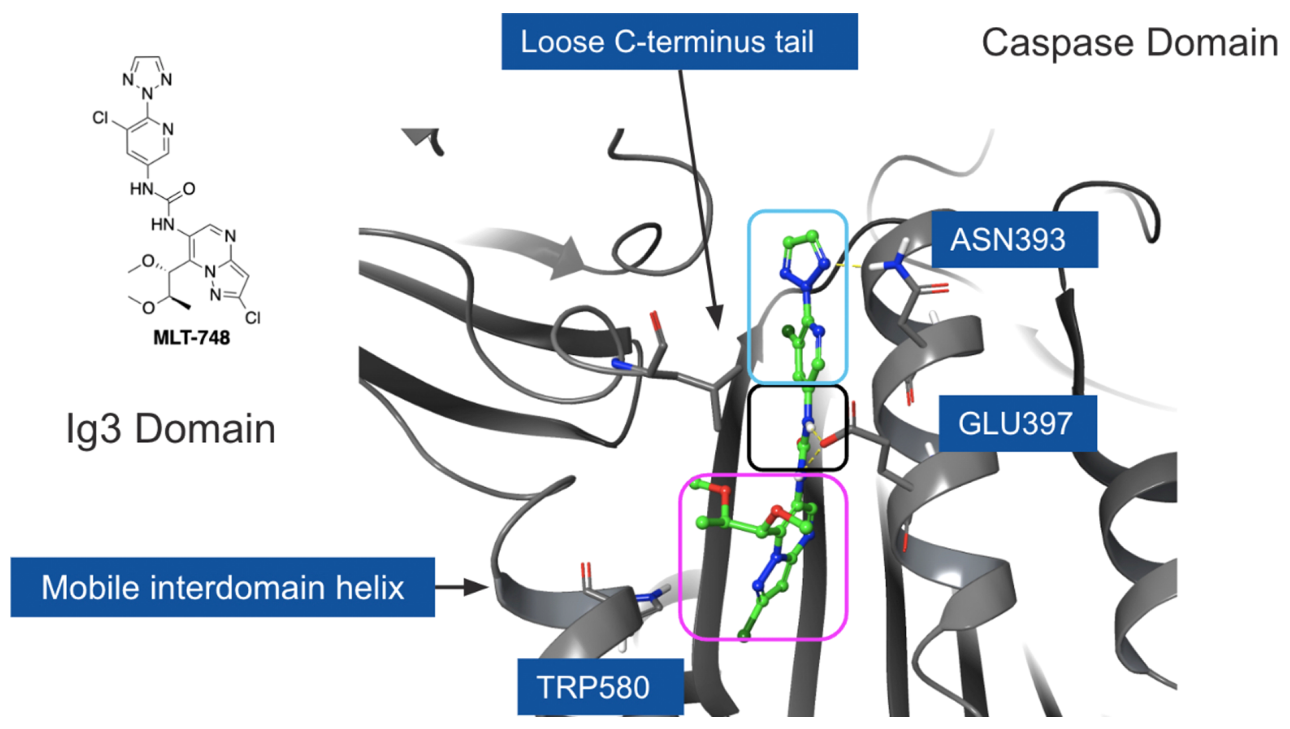
图注:MLT-748与MALT1形成复合物的共晶结构(PDB ID:6H4A)(紫红色为Core 1,黑色为Linker,蓝色为Core 2)
首先,研究团队利用已知MALT1抑制剂的共晶结构,构建并验证了可靠的自由能微扰(FEP+)模型,实现了对配体结合亲和力的精准预测。FEP+是一种预测分子相对结合能的计算方法,其准确性与实用性已得到充分验证,预测结果与实验值的偏差平均可控制在1 kcal/mol内。
研究团队对现有化学物质进行了构效关系(SAR)分析,随后利用WaterMap(水分子热力学分析)对别构结合位点展开计算评估。结果显示,结合位点的特定区域有多个可置换的高能水分子。这一发现不仅为提升分子活性提供了可能,也为探索不同化学类型创造了条件。
基于此,研发团队采用“从头设计”(De Novo Design)策略,通过FEP+技术(基于OPLS4力场)进行大规模迭代设计与评分,对数十亿个化合物进行了评估。下图显示了新型MALT1抑制剂设计策略:初始阶段保持Core 2区域不变,对Linker和Core 1区域进行多种结构修饰。
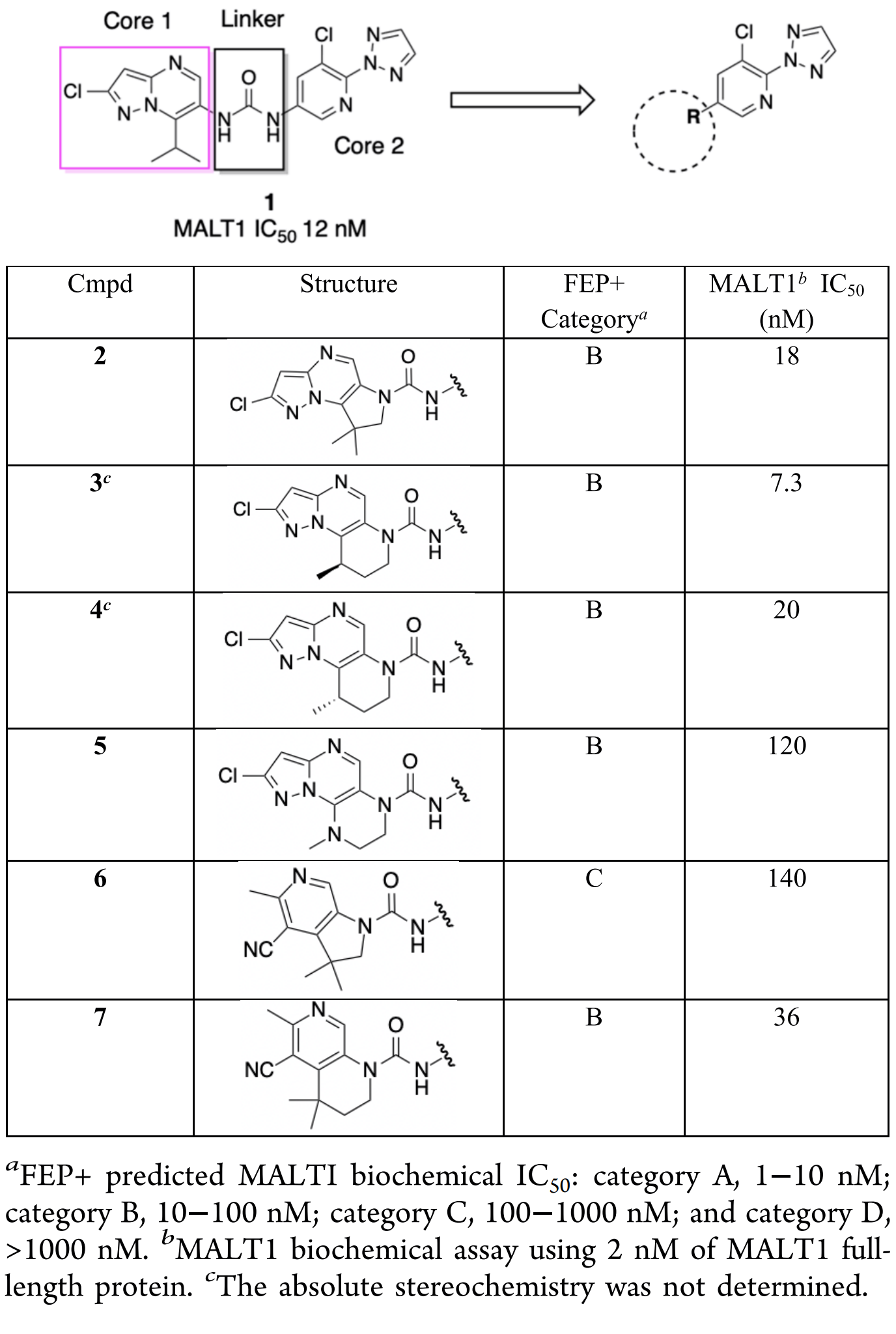
图注:FEP+驱动的De Novo设计的SAR
计算枚举或人工设计共生成了约1400个设计方案,初筛和对接实验剔除了不符合结合口袋结构、且/或超出目标理化性质筛选范围的配体。在剩余的方案中,通过完整循环闭合FEP+(full cycle closure FEP+)计算,对约1300个设计方案进行了评估。
基于FEP+活性预测结果,优先选择排名前37的方案进行合成,上表列出了部分化合物的实验数据。此外,别构结合位点的配体结合亲和力(MALT1表面等离子体共振解离常数SPR Kd)与MALT1功能抑制活性(MALT1生化半数抑制浓度IC50)之间存在良好的相关性,这证明了FEP+模型可用于前瞻性地直接预测MALT1的功能抑制效果。
下图所示为化合物2与MALT1形成复合物的共晶结构,分辨率达2.45 Å。在MALT1别构结合位点中,化合物2的结合构象与文献化合物1的结合构象高度重叠。化合物1的脲基连接链可与GLU397残基形成两个关键氢键相互作用(紫红色标注),而新设计的化合物2仅通过一个氨基(NH)与该残基形成氢键相互作用(黄色标注),并仍保持了与参考化合物相近的MALT1抑制活性。FEP+模型精准预测了“单个氢键相互作用即可维持活性”这一结论,且该预测结果已通过实验数据得到验证。
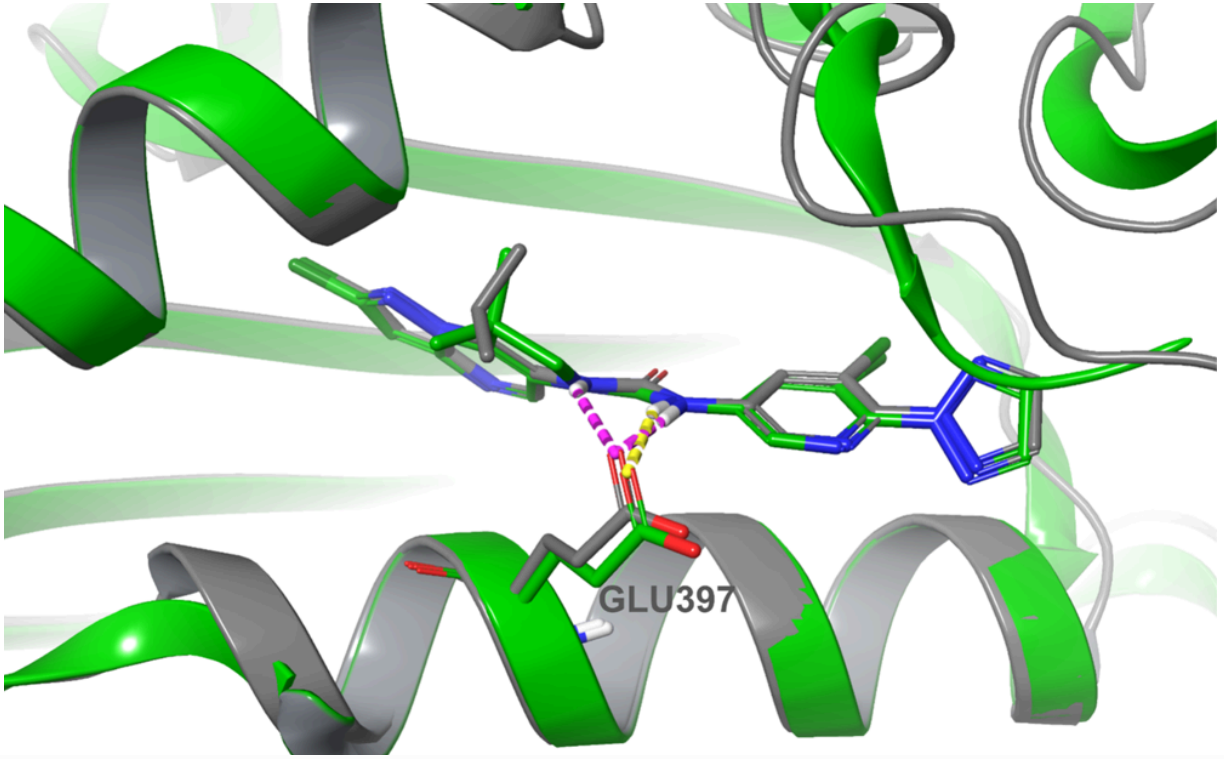
图注:化合物1(灰色)和化合物2(绿色)分别与MALT1形成复合物的共晶结构叠加图(PDB ID:9MKC和9MKD)
总之,通过将FEP+与高性能云计算、机器学习(即主动学习FEP+)相结合,研究人员得以迅速完成对数以千计分子的评估,成功识别出全新且独特的高活性MALT1抑制剂系列(即三环脲类化合物系列),为后续开发奠定了基础。
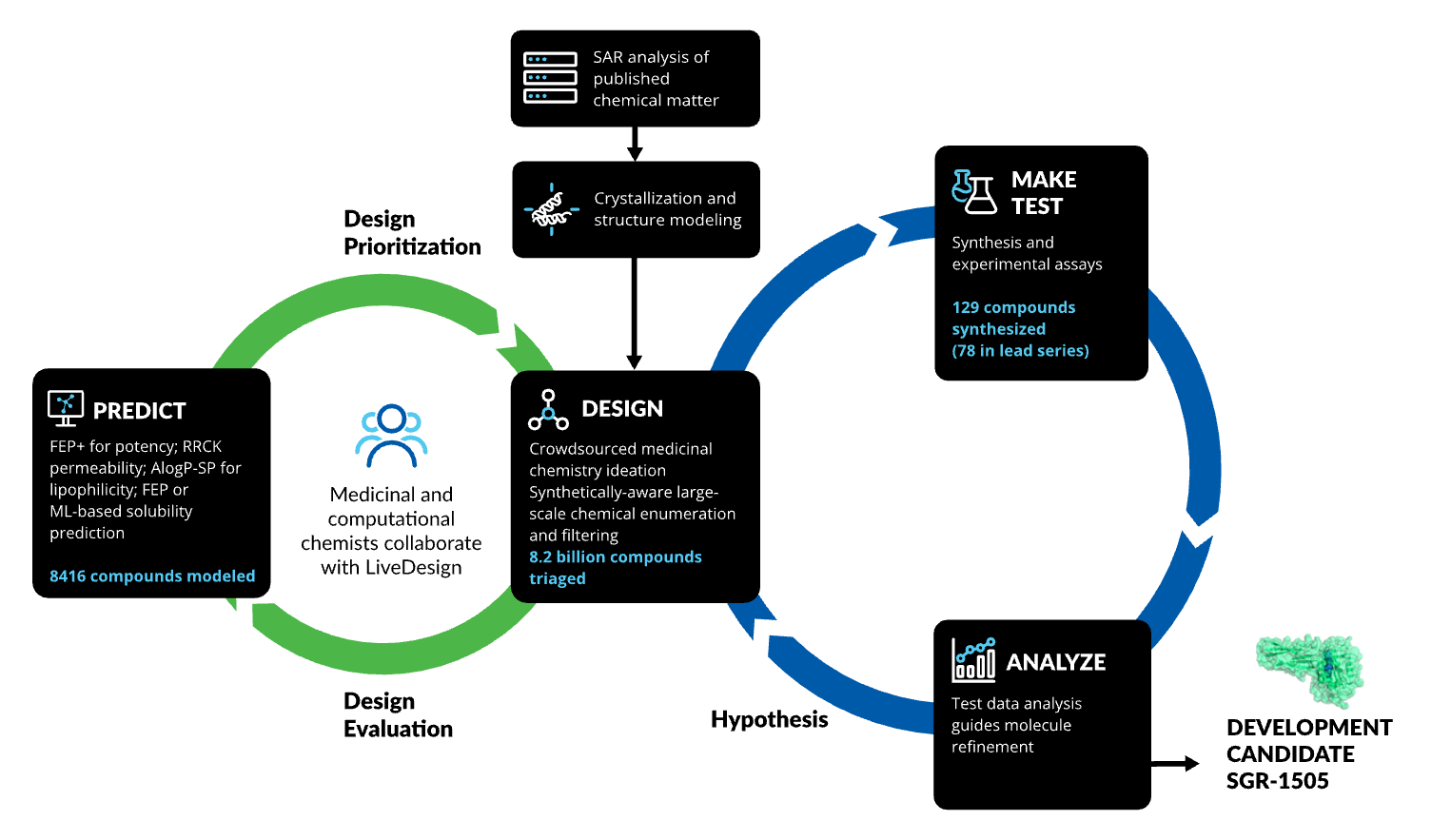
图注:MALT1抑制剂项目采用的建模策略与设计-预测-合成-测试-分析(DPMTA)循环
识别到极具潜力的化合物后,如何对其进行进一步优化呢?敬请关注下一篇。
参考资料
1. Nie, Zhe et al. “Accelerated In Silico Discovery of SGR-1505: A Potent MALT1 Allosteric Inhibitor for the Treatment of Mature B-Cell Malignancies.” Journal of medicinal chemistry, 10.1021/acs.jmedchem.5c01494. 13 Oct. 2025, doi:10.1021/acs.jmedchem.5c01494
2. A Phase 1 study of SGR-1505, an oral, potent, MALT1 inhibitor for relapsed/refractory (R/R) B-cell malignancies, including chronic lymphocytic leukemia/small lymphocytic leukemia (CLL/SLL). Spurgeon, et al. European Hematological Association Annual Congress. 2025.
3. Hit to development candidate in 10 months: Rapid discovery of SGR- 1505, a novel, potent MALT1 inhibitor, Schrödinger



