掺杂空位协同影响Ag2O颗粒光催化抗生素降解研究
关键词:抗生素降解、环丙沙星、光催化、Ag2O、DFT
1.案例背景
随着现代分析技术的发展和人们环境安全意识的增强,抗生素等新兴有机污染物在自然水环境中的出现已引起广泛关注。环丙沙星(CIP)就是抗生素污染物的其中之一。人类长期饮用被CIP污染的水源会出现腹痛、腹泻、头痛、头晕等不良反应。因此为了降低此类抗生素在环境中的浓度,科研人员利用光催化技术对CIP进行降解。寻找高效的光降解催化剂成了此类研究的重中之重。为了在光催化中利用更多的光辐射,小带隙半导体是研究的重点,Ag2O即为此类材料,其带隙为1.2-1.4eV。但因Ag2O纳米颗粒的光稳定性较差,需要通过改性调节Ag2O的电荷转移,来转移或减少此类问题。本案例作者通过水热法制备了Ni掺杂的Ag2O纳米颗粒,并且材料中含有一定量的O空位。Ni掺杂和O空位的协同效应改善了Ag2O费米能级附近的能带结构,增强了电荷分离效率,促进了CIP的降解。最后作者使用DFT计算验证了实验观点,并推测了可能的降解机理。
2.建模与计算方法
作者通过MedeA InfoMaticA 搜索了Ag2O晶胞。使用Supercell Builder扩胞得到Ag2O-2×2×2超胞;而后分别使用Substitutional search和Find empty space创建了Ni取代Ag掺杂和Ni空位掺杂的Ag2O超胞,并在结构中引入了一定的氧空位。随后采用MedeA-VASP模块中的DFT对结构进行优化和电子性质计算,截断能选取400 eV,K点基矢选取4×4×4,最后计算结合实验推测了光催化降解的机理。
3.结果与讨论
3.1 实验部分:
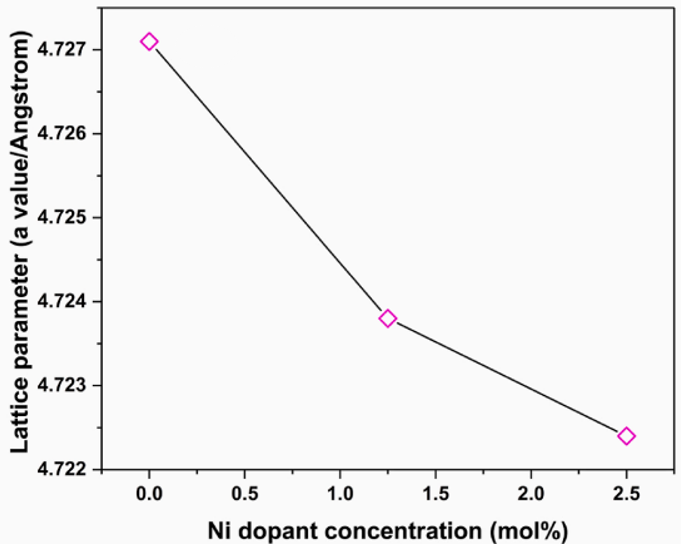
图1 Ag2O纳米颗粒的晶格随着Ni掺杂剂摩尔百分比的增加变化图。
作者通过水热法合成了Ag2O纳米颗粒,并用Ni进行掺杂,得到了不同Ni掺杂剂比例的Ag2O,并按照1.25、2.5、5摩尔百分比命名为N1、N2、N3,纯Ag2O为N0。通过X射线衍射(XRD),投射电子显微镜(TEM),X射线电子能谱(XPS)等验证了材料的成功合成,但在N3中发现了新产生的NiO相,所以在之后并未对N3进行更多的研究。随后分析了Ni掺杂Ag2O的晶体结构。Ni2+和Ag+的有效离子半径分别为69 p.m.和115 p.m.,这说明掺杂剂中的Ni原子能够占据Ag2O晶胞中的间隙位置或取代Ag原子。半径较小的Ni原子取代半径较大的Ag原子,晶格会发生收缩。Ni占据较小的间隙位置晶格将会增大。图1显示了Ag2O晶格参数随掺杂剂浓度的变化而变化。随着Ni掺杂剂浓度的上升,Ag2O的晶格随之收缩。显然掺杂剂中的Ni会取代Ag,在Ag2O中进行掺杂。
而后作者结合X射线电子能谱(XPS)分析了材料的能隙信息。如图2a所示,曲线线性部分的切线切割x轴,表示材料带隙能量值(eV),样品N0、N1和N2的带隙值分别为1.53、1.43和1.4 eV。带隙随Ni掺杂浓度的上升而减小。N2具有三个样品中最小的带隙(1.4 eV)。图2b显示了N0和N2样品的VB-XPS光谱。VB-XPS的x轴截距表示VB位置,N0=0.8 eV,N2=0.87 eV。N2的VB位置略微偏移,移动到了比N0更正的值。样品N0和N2的CB边缘分别为-0.73和-0.53eV。N2样品的CB比N0样品更负,偏移达到0.2eV。随后为了更深入地研究氧空位和Ni掺杂的协同性质,进行密度泛函理论(DFT)计算。
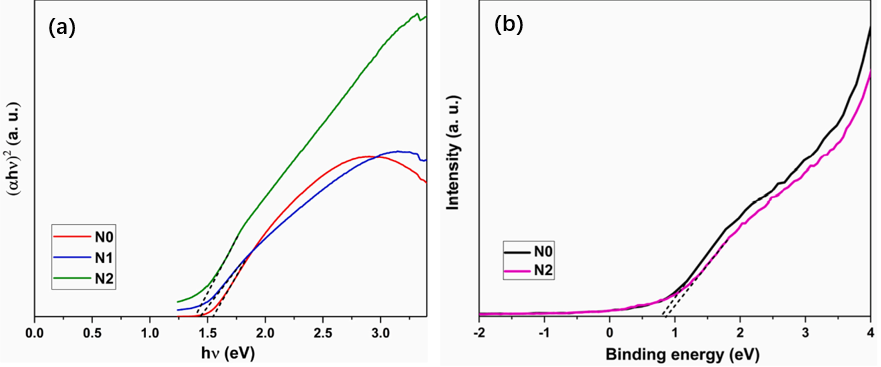
图2 (a)N0、N1、N2的XPS图(b)N0和N2的VB-XPS图
3.2 理论计算部分
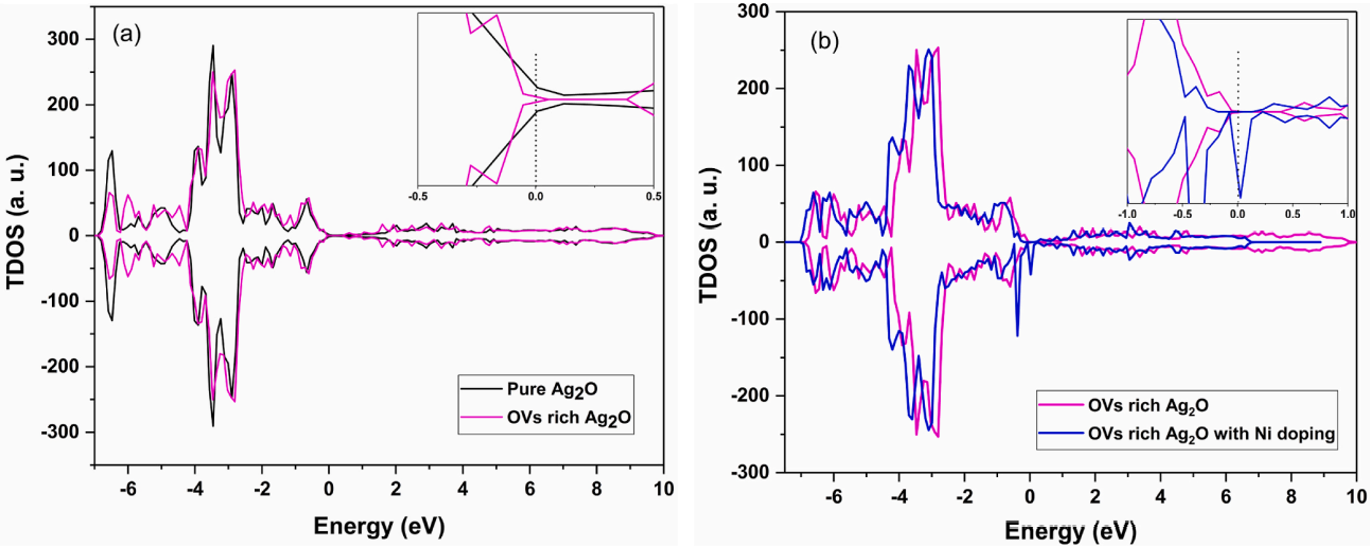
图3 (a)纯Ag2O和富OV的Ag2O的总态密度(TDOS)的比较。(b)富含OV的Ag2O和Ni掺杂Ag2O的总态密度(TDOS)的比较。
为深入了解OV和Ni掺杂对Ag2O的影响,作者通过MedeA-VASP对其进行了DFT计算分析。首先计算了Ni原子取代Ag的位置和占据间隙位置的形成能。Ni掺杂取代Ag体系的形成能为0.18eV,而间隙掺杂体系的形成能量为1.09eV。因此,Ag2O结构中的Ni掺杂取代Ag在能量方面明显更有利,并与先前讨论的实验发现一致。
随后作者在Ag2O引入OV,并计算了引入OV前后的Ag2O的态密度。图3a显示了纯Ag2O和富含OV的Ag2O的总态密度(TDOS)的对比。纯Ag2O的TDOS显示其没有带隙,在引入OV后带隙为0.5eV。这说明O空位的引入能改善Ag2O的电子结构,有助于电荷的有效分离。图3b展示的是在富含OV的Ag2O中引入Ni掺杂前后计算得到的TDOS的对比。在Ni掺杂之后禁带区域出现新的掺杂能级,从而使得富含OV的Ag2O的TDOS显示没带隙值。但是掺杂能级能够作为价带电子跃迁的平台,从而有效加速电荷的转移。并且能观察到富含OV和Ni掺杂的Ag2O的CB有效区(从CB最小值到CB最大值)从9.8eV转变到6.7eV,而VB从6.7eV转变为6.9eV,与先前的实验发现一致。
3.3 机理推测
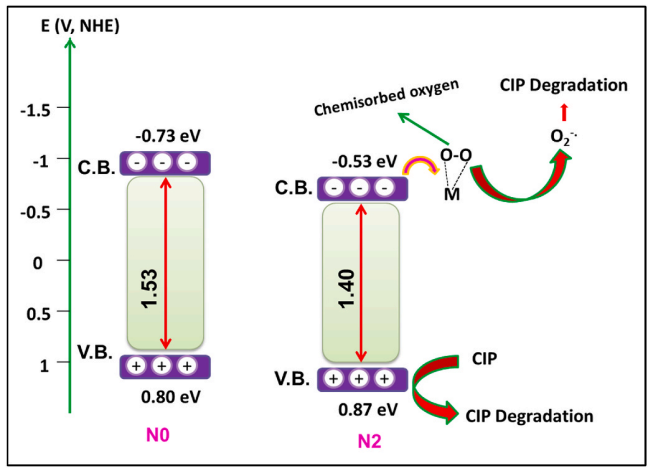
图4 CIP光降解机理推测示意图。
图4为光催化CIP降解机理推测示意图。通过实验和DFT模拟得到,OV的存在使得Ag2O纳米颗粒的带隙(1.53eV)变宽。OV-Ag2O体系中的Ni掺杂将带隙降低到1.4eV,并且还改变了VB和CB带位置。在用可见光照射光催化剂时,电子从其VB被光激发到CB。OVs可以捕获这种光激发的电子并将其转移到化学吸附的氧中,形成超氧自由基,从而形成其他活性氧物种,将会加速CIP的降解。光催化剂的VB位置也至关重要。由于N2具有比N0更正的VB位置,所以在VB上氧化CIP的效果会更加明显。
4.总结与展望
本案例中,作者通过水热法合成了Ag2O纳米颗粒,具有1.53eV的带隙。XPS分析和DFT计算表明,引入O空位会使Ag2O的带隙增大。掺杂Ni会降低纳米颗粒中的OV浓度,同时注入了额外的电子,增加了化学吸附氧的百分比。价带XPS分析表明,Ni掺杂后材料显示出更负的CB和更正VB,DFT计算也证明了定性相似的结果。Ni掺杂Ag2O体系表现出更快的CIP降解速率。最后推测了光催化降解CIP的机理,为能带结构工程提供了新的见解,为环境净化的研究做出了贡献。
参考文献:
A. De, I. Sinha. Synergistic effect of Ni doping and oxygen vacancies on the visible light photocatalytic properties of Ag2O nanoparticles, Journal of Physics and Chemistry of Solids 167 (2022) 110733
使用模块:
MedeA Environment
MedeA VASP



