1.研究背景
HIV-1 融合抑制剂是继逆转录酶和蛋白酶抑制剂后的新一类抗 HIV感染药物, 通过阻断病毒与靶细胞膜的融合从而抑制病毒进入靶细胞, 在感染的初始环节切断 HIV-1 的传播, 其中多肽类融合抑制剂 T-20 已于2003 年上市。HIV-1 融合抑制剂以 HIV-1 跨膜糖蛋白gp41 为作用靶标, 它们是一些天然或合成的多肽以及小分子化合物, 通过与 gp41 功能区结合从而抑制其促融合功能的发挥。近年来, 随着对膜融合过程分子机制以及gp41 功能研究的不断深入, 新的以 gp41 不同功能区为靶点的融合抑制剂分子不断被发现, 成为倍受关注的研究热点之一。
2.研究流程
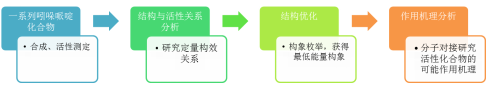
图1 实验流程
研究合成了一系列吲哚哌啶类化合物,然后进行活性测定。基于活性测定结果对化合物进行了定量构效关系研究。然后对化合物进行构象枚举得到最低能量构象以后进行了分子对接。
3.研究结果
研究合成了一系列吲哚哌啶类化合物,该类化合物具有A-D 4个芳香环结构。芳香环的存在,有利于增强化合物结构的疏水性,提高与靶标蛋白的亲和力。研究对合成的化合物进行了生物活性测定,又结合活性与结构的关系深入分析了化合物的定量构效关系。研究又深入分析了化合物与靶标作用时的可能构象(图3),分析发现化合物表现出来的对接打分与其生物活性呈正相关。其中化合物6j和6k的对接打分最高,并且表现出较好的生物活性。因此表明,研究通过计算得到的化合物结合构象可能是其发挥生物活性的构象。这为下一步化合物结构优化及改造提供指导。
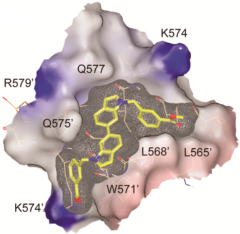
图2 化合物6j和靶蛋白的相互作用图
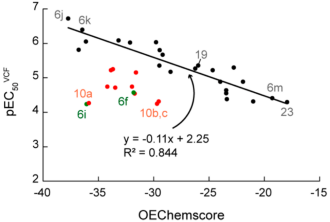
图3 对接结果与活性值之间的相关性
4.结论
研究合成了一系列吲哚哌啶化合物,并进行了生物活性测定。接着对化合物进行了定量构效关系研究,发现化合物结构的形状和电荷性质可以提高其与靶蛋白的结合亲和力。研究发现化合物6j与蛋白的结合亲和力最高,Ki值为0.6 mM。并且化合物6j表现出良好的靶蛋白抑制活性,抑制中浓EC50为0.2 mM。研究又进行了分子对接,分析化合物与靶蛋白可能的相互作用机理。使用构象采样的方法获得化合物可能的活性构象,然后进行分子对接。分析对接结果发现抑制活性较好的化合物都结合在靶蛋白gp41的卷曲螺旋上的疏水口袋。通过分析发现,增加化合物的脂溶性会有利于其与膜蛋白gp41的结合,更有利于提高抑制活性。这一发现将为化合物结构的进一步优化提供指导。
使用模块:
OMEGA
ROCS
FRED
参考文献:
1. Zhou G, Wu D, Snyder B, et al. Development of Indole Compounds as Small Molecule Fusion Inhibitors Targeting HIV-1 Glycoprotein-41[J]. Journal of Medicinal Chemistry, 2011, 54(20): 7220-7231.



