 |
|
 |
|
新建计算机化 系统验证服务 |
遗留计算机化系统 合规验证服务 |
|
|
|
|
|
 |
|
|
|
验证培训与咨询 |
|
|
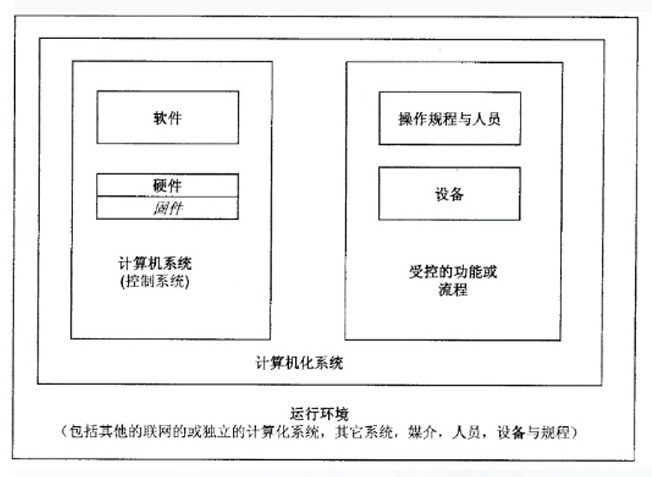
 |
|
|
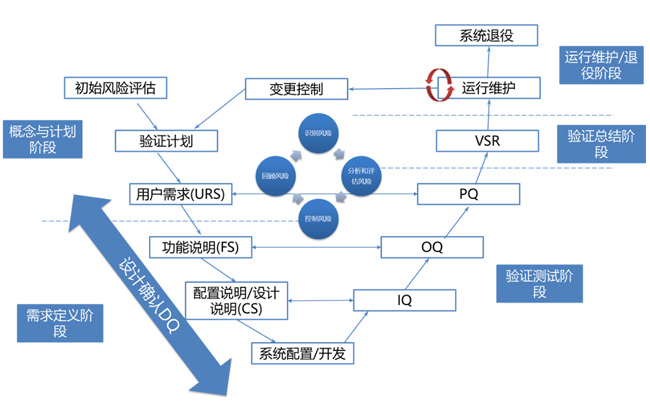
计算机化系统验证V-model |
|
|
|
|
 |
|
|
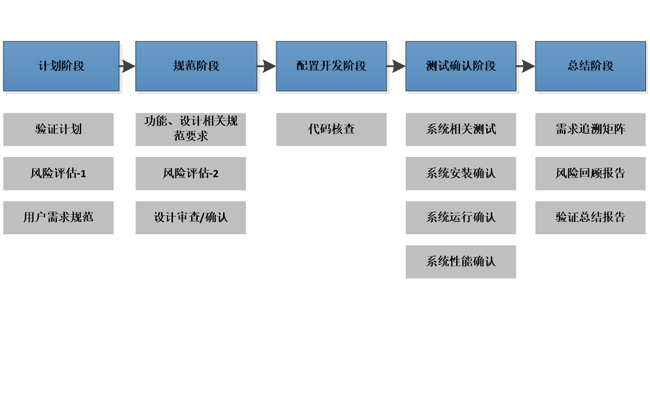
验证与交付流程 |
|